Сплавы
Разного рода добавки могут использоваться и специально для повышения прочности такого пластичного материала, как медь. Электропроводность ее они также снижают. Но зато их применение позволяет значительно продлить срок службы разного рода изделий.

Чаще всего в качестве повышающей прочность меди добавки используется Cd (0.9 %). В результате получается кадмиевая бронза. Ее проводимость составляет 90 % от проводимости меди. Иногда вместо кадмия в качестве добавки используют также алюминий. Проводимость этого металла составляет 65 % от этого же показателя меди. Для повышения прочности проводов в виде добавки могут применяться и другие материалы и вещества — олово, фосфор, хром, бериллий. В результате получается бронза определенной марки. Соединение меди с цинком называется латунью.
Общая минерализация
Устройства для измерения удельной электрической проводимости часто используют для определения общей минерализации или содержания твёрдых веществ
(англ. total dissolved solids, TDS). Это мера общего количества органических и неорганических веществ, содержащихся в жидкости в различных формах: ионизированной, молекулярной (растворенной), коллоидной и в виде суспензии (нерастворенной). К растворенным веществам относятся любые неорганические соли. Главным образом, это хлориды, бикарбонаты и сульфаты кальция, калия, магния, натрия, а также некоторые органические вещества, растворенные в воде. Чтобы относиться к общей минерализации, вещества должны быть или растворенными, или в форме очень мелких частиц, которые проходят сквозь фильтры с диаметром пор менее 2 микрометров. Вещества, которые постоянно находятся в растворе во взвешенном состоянии, но не могут пройти сквозь такой фильтр, называетсявзвешенными твердыми веществами (англ. total suspended solids, TSS). Общее количество взвешенных веществ обычно измеряется для определения качества воды.

Галерея фильтрации воды на водоочистных сооружениях им. Р. К. Харриса в Торонто, Онтарио, Канада
Существует два метода измерения содержания твердых веществ: гравиметрический анализ
, являющийся наиболее точным методом, иизмерение удельной проводимости . Первый метод — самый точный, но требует больших затрат времени и наличия лабораторного оборудования, так как воду нужно выпарить до получения сухого остатка. Обычно это производится при температуре 180°C в лабораторных условиях. После полного испарения остаток взвешивается на точных весах.
Второй метод не такой точный, как гравиметрический анализ. Однако он очень удобен, широко распространен и является наиболее быстрым методом, так как представляет собой простое измерение проводимости и температуры, выполняемое за несколько секунд недорогим измерительным прибором. Метод измерения удельной электропроводности можно использовать в связи с тем, что удельная проводимость воды прямо зависит от количества растворенных в ней ионизированных веществ. Данный метод особенно удобен для контроля качества питьевой воды или оценки общего количества ионов в растворе.
Измеренная проводимость зависит от температуры раствора. То есть, чем выше температура, тем выше проводимость, так как ионы в растворе при повышении температуры движутся быстрее. Для получения измерений, независимых от температуры, используется концепция стандартной (опорной) температуры, к которой приводятся результаты измерения. Опорная температура позволяет сравнить результаты, полученные при разных температурах. Таким образом, измеритель удельной проводимости может измерять реальную проводимость, а затем использовать корректирующую функцию, которая автоматически приведет результат к опорной температуре 20 или 25°C. Если необходима очень высокая точность, образец можно поместить в термостат, затем откалибровать измерительный прибор при той же температуре, которая будет использоваться при измерениях.
Большинство современных измерителей удельной проводимости снабжены встроенным датчиком температуры, который используется как для температурной коррекции, так и для измерения температуры. Самые совершенные приборы способны измерять и отображать измеренные значения в единицах удельной проводимости, удельного сопротивления, солености, общей минерализации и концентрации. Однако еще раз отметим, что все эти приборы измеряют только проводимость (сопротивление) и температуру. Все физические величины, которые показывает дисплей, рассчитываются прибором с учетом измеренной температуры, которая используется для автоматической температурной компенсации и приведения измеренных значений к стандартной температуре.
Интересные факты об алюминии

Алюминиевый корпус внешнего аккумулятора для телефона. Экструдированный анодированный окрашенный профиль.
Алюминий весьма посредственно паяется мягкими (оловянно-свинцовыми) припоями, неплохо паяется цинковыми припоями. При конструировании приборов это стоит помнить, соединить провод с алюминиевым шасси проще прикрутив винтом к запрессованной стойке, чем припаять. В твердых марках алюминия (6061, 6082, 7075) можно нарезать резьбу для винта непосредственно.
Алюминий можно сваривать аргоновой сваркой, но качественный шов получается только при TIG-сварке на переменном токе. Непрерывная смена полярности измельчает пленку окислов, которая в противном случае может попасть в шов. Учитывайте это при выборе сварочного аппарата для мастерской, если вам может потребоваться варить и алюминий.
Еще раз важное замечание. Алюминиевые и медные проводники напрямую соединять нельзя! Для соединения проводников из меди и алюминия используйте промежуточный металл, например, стальную клемму
Источники
Вольфрам — не очень пластичный материал, поэтому спиральку из лампы накаливания вряд ли удастся выпрямить и использовать по своему разумению. Если вдруг понадобится вольфрамовый стержень — вам пригодится любой магазин по сварочному делу, электрод для TIG-горелки без содержания лантана и других присадок. Проволоку для нитей накала самодельной техники нетрудно купить на eBay.
- Цветовая маркировка электродов:
- Зеленый — чистый вольфрам.
- Красный, оранжевый — вольфрам + торий. Радиоактивно! Не шлифовать, не резать — пыль опасна!
- Голубой — вольфрам + сложная смесь.
- Черный, желтый, синий — вольфрам + лантан.
- Серый — вольфрам + церий.
- Белый — вольфрам + цирконий.
Соединения меди
Оксид меди (I) Cu2O3 и закись меди (I) Cu2O, как и другие соединения меди (I) менее устойчивы, чем соединения меди (II). Оксид меди (I), или закись меди Cu2O в природе встречается в виде минерала куприта. Кроме того, она может быть получена в виде осадка красного оксида меди (I) в результате нагревания раствора соли меди (II) и щелочи в присутствии сильного восстановителя.
Оксид меди (II), или окись меди, CuO — черное вещество, встречающееся в природе (например в виде минерала тенерита). Его получают прокаливанием гидроксокарбоната меди (II) (CuOH)2CO3 или нитрата меди (II) Cu(NO2)2. Оксид меди (II) хороший осислитель.
Гидроксид меди (II) Cu(OH)2 осаждается из растворов солей меди (II) при действии щелочей в виде голубой студенистой массы. Уже при слабом нагревании даже под водой он разлагается, превращаясь в черный оксид меди (II). Гидроксид меди (II) — очень слабое основание. Поэтому растворы солей меди (II) в большинстве случаев имеют кислую реакцию, а со слабыми кислотами медь образует основные соли.
Сульфат меди (II) CuSO4 в безводном состоянии представляет собой белый порошок, который при поглощении воды синеет. Поэтому он применяется для обнаружения следов влаги в органических жидкостях. Водный раствор сульфата меди имеет характерный сине-голубой цвет. Эта окраска свойственна гидратированным ионам 2+, поэтому такую же окраску имеют все разбавленные растворы солей меди (II), если только они не содердат каких-либо окрашенных анионов. Из водных растворов сульфат меди кристаллизуется с пятью молекулами воды, образуя прозрачные синие кристаллы медного купороса. Медный купорос применяется для электролитического покрытия металлов медью, для приготовления минеральных красок, а также в качестве исходного вещества при получении других соединений меди. В сельском хозяйстве разбавленный раствор медного купороса применяется для опрыскивания растений и протравливания зерна перед посевом, чтобы уничтожить споры вредных грибков.
Хлорид меди (II) CuCl2. 2H2O. Образует темно-зеленые кристаллы, легко растворимые в воде. Очень концентрированные растворы хлорида меди (II) имеют зеленый цвет, разбавленные — сине-голубой.
Нитрат меди (II) Cu(NO3)2.3H2O. Получается при растворении меди в азотной кислоте. При нагревании синие кристаллы нитрата меди сначала теряют воду, а затем легко разлагаются с выделением кислорода и бурого диоксида азота, переходя в оксид меди (II).
Гидроксокарбонат меди (II) (CuOH)2CO3. Встречается в природе в виде минерала малахита, имеющего красивый изумрудно-зеленый цвет. Искусственно приготовляется действием Na2CO3 на растворы солей меди (II). 2CuSO4 + 2Na2CO3 + H2O = (CuOH)2CO3v + 2Na2SO4 + CO2^ Применяется для получения хлорида меди (II), для приготовления синих и зеленых минеральных красок, а также в пиротехнике.
Ацетат меди (II) Cu (CH3COO)2.H2O. Получается обработкой металлической меди или оксида меди (II) уксусной кислотой. Обычно представляет собой смесь основных солей различного состава и цвета (зеленого и сине-зеленого). Под названием ярь-медянка применяется для приготовления масляной краски.
Комплексные соединения меди образуются в результате соединения двухзарядных ионов меди с молекулами аммиака. Из солей меди получают разноообразные минеральные краски. Все соли меди ядовиты. Поэтому, чтобы избежать образования медных солей, медную посуду покрывают изнутри слоем олова (лудят).
Токопроводящий клей своими руками
Многие начинающие радиолюбители задаются вопросом, как сделать токопроводящий клей своими руками. Здесь необходимо внести ясность в некоторые вопросы, которые новички задают чаще всего.
- Проводит ли ток клей момент? Это клей, который был разработан и представлен немецкой компанией Хенкель. Всего было создано 6 составов для различных целей, но ни один из них не проводит ток.
- Проводит ли супер клей электричество? Чтобы ответить на этот вопрос, необходимо обратиться к самому понятию электропроводящего материала. Супер клей не содержит компонентов, которые позволили бы назвать его электропроводным (графит, металлы), поэтому его показатели в этом плане практически не отличаются от пластмассы.
- Проводит ли эпоксидный клей электричество? Эпоксидная смола не проводит электрический ток по вышеуказанной причине.
- Можно ли ремонтировать при помощи такого клея провод высокого напряжения? Мастера не рекомендуют этого делать, так как это идет вразрез с правилами безопасности при работе с электричеством.
- Почему контактол не работает? В современное время появилось очень много подделок этого клея, поэтому лучше приобретать этот клей с гарантиями от производителя.
- Какой клей проводит электрический ток? Любой клей, в состав которого входят электропроводящие компоненты в достаточном объеме.
Инструкция по изготовлению
В последнее время радиолюбители нелестно отзываются о современных производителях токопроводящего клея. Быть может, все дело в подделках или сами производители предоставляют некачественный товар. К тому же, токопроводящий клей для микросхем и другого оборудования иногда нужен срочно, и времени на его приобретение или заказ нет. В таком случае можно изготовить такой состав самостоятельно, воспользовавшись нашей инструкцией.
Как сделать токопроводящий клей? Для начала необходимо запастись необходимым набором материалов. Он довольно скромен:
- графитовый стержень от строительного или простого карандаша, который и будет выступать основным токопроводящим элементом в получившемся составе;
- канцелярский нож;
- лист бумаги для сбора графитной пыли;
- молоток;
- емкость для сбора графитной пыли;
- лак для ногтей.
Для начала вам необходимо получить графитный стержень. При помощи канцелярского ножа сточите деревянную часть карандаша до такого состояния, когда графитный стержень можно будет вынуть. После этого положите стержень на лист бумаги, закройте его так, чтобы пыль не разлетелась в стороны и молотком измельчите грифель до состояния пыли. Эта пыль и станет токопроводящим элементом. Соберите пыль в емкость (для этого отлично подойдет обыкновенная крышка от пластиковой бутылки). Налейте в емкость лак для ногтей и тщательно перемешайте с графитной пылью при помощи деревянных палочек, которые могли остаться после обработки карандаша. Теперь токопроводящий клей готов! Удобство этого клея в том, что у вас есть право на ошибку. Лак для ногтей легко удаляется при помощи специального состава.
В народе известны также составы, которые используют в своей основе металлическую крошку или пыль. Можно включить воображение и вспомнить школьный курс химии и физики, где говорилось о токопроводящих материалах. Приведем пример. Графит – это по своей сути углерод с характерной кристаллической решеткой. Углерод также содержится в продуктах горения дерева – в саже. По этой причине токопроводящий клей с сажей также является довольно популярным среди радиолюбителей.
Особенности самодельного клея
- Никто не застрахован от ошибок. Когда вы что-либо делаете своими руками, вы рискуете сделать что-то не так, в результате чего можно повредить дорогостоящее оборудование. Поэтому в некоторых случаях лучше доверить профессионалам и потратиться на приобретение фирменного состава.
- Надежность клея на основе лака для ногтей не так высока, как у покупного клея. Помните о том, что такой лак не будет служить вам вечно и рано, и его ресурс прочности закончится довольно скоро.
- Лак для ногтей довольно долго высыхает, по сравнению с покупными аналогами.
- Самодельный токопроводящий клей гораздо дешевле в изготовлении.
- Процесс изготовления занимает меньше 3 минут, что не сильно тормозит рабочий процесс.
Все эти факты говорят о том, что лучше всего приобрести однажды фирменный токопроводящий клей и пользоваться им долгое время, чем каждый раз делать свой состав, который будет быстро выходить из строя.
Токопроводящий клей – отличное средство для тех, кому необходимо быстро и эффективно осуществить ремонт электрооборудования. И только вам решать, изготовить клей самостоятельно или купить зарекомендованную марку.
Какое удельное сопротивление стали
Сталь — это металлический сплав железа с углеродом и другими элементами. В ее состав входит не менее 45% железа, содержание углерода колеблется от 0,02% до 2,14%. В зависимости от точного состава сталь используется в строительстве, машиностроении и приборостроении, а также во многих областях, например, в транспорте, народном хозяйстве, при производстве бытовых приборов.

Проводимость стали составляет всего 7,7 миллионов См/м, удельное сопротивление — 0,13 мкОм/м, то есть оно довольно высоко. Сталь плохо проводит электричество и не применяется при производстве непосредственно кабелей. Однако нередко можно встретить внешнюю оцинкованную стальную оплетку, которая защищает провода от механического растяжения. Такая защита нужна, если кабель проходит под дорогой или на нестабильном грунте, если есть риск резко дернуть провод.
Также из стали делают ПНСВ — провод нагревательный со стальной жилой, имеющий изоляцию из винила. Его размещают внутри конструкции до заливания бетона и используют в дальнейшем для электрообогрева готового блока. Электричество кабель практически не проводит.

2.1.1. Физическая природа электропроводности металлов
Металлы имеют кристаллическое строение: в узлах кристаллической решетки находятся положительно заряженные ионы, окруженные коллективизированными электронами (электронным газом).
Современные представления об электронном строении металлов, распределении электронов по энергетическим состояниям, их взаимодействии с другими элементарными частицами и кристаллической решеткой дает квантовая теория, основы которой были разработаны советским ученым Я.И.Френкелем и немецким физиком А.Зоммерфельдом.
Читать также: Добыча цветных металлов в мире
Свободные электроны хаотически перемещаются по кристаллу со средней тепловой скоростью и = 10 5 м/с. В электрическом поле напряженностью Е электроны получают добавочную скорость упорядоченного движения v – скорость дрейфа, благодаря чему и возникает электрический ток. Плотность тока зависит от скорости дрейфа, заряда электрона е и концентрации свободных электронов n .
Скорость дрейфа в реальных условиях существенно меньше скорости теплового движения электронов v u . Так, в медном про-
воднике при плотности тока j = 1 А/мм 2 скорость дрейфа составляет v = 1 . 10 -4 м/с.
За время τ между столкновениями с узлами кристаллической решетки на длине свободного пробега l , электроны, двигаясь с уско-
рением a = e E , приобретают скорость дрейфа: m e
Приравнивая аналитическое выражение закона Ома (1.1) к выражению (2.1) с учетом (2.2), получим формулу для удельной проводимости
Выразим произведение m e . и через концентрацию свободных электронов, используя квантовую статистику, базирующуюся на принципе Паули, согласно которому в каждом энергетическом состоянии может находиться только один электрон, а на каждом энергетическом уровне – не более двух (с антипараллельными спинами). Тогда при температуре абсолютного нуля ( Т = 0 К) половина из общего числа свободных электронов в кристалле ( n /2) займет наиболее низкие энергетические уровни.
В квантовой теории вероятность заполнения электронами энергетических состояний с энергией уровня Э определяется функцией Ферми
где Э F – энергия Ферми, т.е. максимальная энергия, которую может иметь электрон в металле при температуре абсолютного нуля.
Из формулы (2.4) следует, что при Э = Э F , вероятность заполнения электронами уровня Ферми равна 0,5. Энергия Ферми для большинства металлов составляет от 3 до 15 эВ. Уровни, расположенные ниже уровня Ферми ( Э Э F ), с вероятностью >0,5 заполнены электронами, а уровни, лежащие выше уровня Ферми ( Э > Э F ), с такой же вероятностью свободны от электронов.
В соответствии с квантовой статистикой Ферми-Дирака концентрация свободных электронов в металле определяется путем интег-
рирования по всем заполненным энергетическим состояниям, что дает следующее выражение
Выразив из этого соотношения значение энергии Ферми через концентрацию электронов и, учитывая, что Э F = m e и 2 2 , получим
Подставляя m e и в формулу (2.3), найдем выражение для
удельной проводимости металлов
Концентрация свободных электронов в чистых металлах, характер их распределения по энергиям и энергия Ферми с повышением температуры почти не изменяются. Например, при нагреве серебра от 0 до 1000 К энергия Ферми уменьшается лишь на 0,2%. Такие малые изменения в широком температурном диапазоне можно не учитывать. Следовательно, формула (2.6) справедлива при любой температуре. Поэтому электропроводность металла определяется, в основном, средней длиной свободного пробега электронов, которая зависит от электронного строения атомов и типа кристаллической решетки. Длина свободного пробега для некоторых металлов дана в табл. 1.
Длина свободного пробега электронов в некоторых металлах при 0 ° С
Наибольшая длина свободного пробега наблюдается в металлах с гранецентрированной кубической кристаллической решеткой (Ag, Cu, Au), которые и являются лучшими проводниками.
Переходные металлы (Fe, Ni, Co, Cr, Mn, V, Zr, Nb, Mo, W, Hf, Ta, Re, Pt и др.) имеют меньшую электропроводность, что связано с их специфическим электронным строением. В этих элементах внутренние d – или f -оболочки неполностью заполнены электронами. В электрическом поле часть валентных электронов из внешней s – оболочки переходят на свободные уровни внутренних оболочек, что приводит к уменьшению числа свободных электронов, участвующих в проводимости.
Особенности электронного строения переходных металлов являются причиной многих их специфических свойств: тепловых, магнитных, склонности к полиморфизму, переменной валентности и др.
И в заключение, у чистых металлов при нагреве средняя энергия электронов практически остается без изменения, что свидетельствует о малой теплоемкости электронного газа.
Технические характеристики
Бескислородная медь обычно указывается в соответствии с базой данных ASTM / UNS . База данных UNS включает множество различных составов электрической меди с высокой проводимостью . Из них три широко используются, а два считаются бескислородными:
- C10100 — также известный как бескислородный электронный (OFE). Это медь чистотой 99,99% с содержанием кислорода 0,0005%. Минимальный рейтинг проводимости по IACS составляет 101% . Эта медь доводится до окончательной формы в тщательно регулируемой бескислородной среде. Серебро (Ag) считается примесью в химической спецификации OFE. Это также самый дорогой из трех перечисленных здесь сортов.
- C10200 — также известный как бескислородный (OF). Хотя OF считается бескислородным, его показатель проводимости не лучше, чем у более распространенного сорта ETP, указанного ниже. Он имеет содержание кислорода 0,001%, чистоту 99,95% и минимальную проводимость 100% IACS. Для определения процента чистоты содержание серебра (Ag) учитывается как медь (Cu).
- C11000 — также известный как электролитическая вязкая смола (ETP). Это самая распространенная медь. Он универсален для электрических применений. ETP имеет минимальный рейтинг проводимости 100% IACS и должен иметь чистоту 99,9%. Он содержит от 0,02% до 0,04% кислорода (типичное значение). Большая часть проданных сегодня ETP соответствует или превышает 101% спецификации IACS. Как и в случае меди OF, содержание серебра (Ag) учитывается как медь (Cu) для целей чистоты.
Бескислородная высокая теплопроводность
Бескислородная медь с высокой теплопроводностью (OFHC) широко используется в криогенике . OFHC производится путем прямого преобразования выбранных очищенных катодов и отливок в тщательно контролируемых условиях, чтобы предотвратить загрязнение чистого бескислородного металла во время обработки. Метод производства меди OFHC обеспечивает очень высокое качество металла с содержанием меди 99,99%. При таком небольшом содержании посторонних элементов свойства элементарной меди проявляются в высокой степени. Этими характеристиками являются высокая пластичность , высокая электрическая и теплопроводность , высокая , хорошее сопротивление ползучести , простота сварки и низкая относительная летучесть в .
Химические свойства
По таким характеристикам медь, электропроводность и теплопроводность которой очень высокие, занимает промежуточное положение между элементами первой триады восьмой группы и щелочными первой группы таблицы Менделеева. К основным ее химическим свойствам относят:
- склонность к комплексообразованию;
- способность давать окрашенные соединения и нерастворимые сульфиды.
Наиболее характерным для меди является двухвалентное состояние. Сходства с щелочными металлами она не имеет практически никакого. Химическая активность ее также невелика. В присутствии СО2 или же влаги на поверхности меди образуется зеленая карбонатная пленка. Все соли меди являются ядовитыми веществами. В одно- и двухвалентном состоянии этот металл образует очень устойчивые комплексные соединения. Наибольшее значение для промышленности имеют аммиачные.
Выбор сечения провода исходя из количества коммуникаций в доме (квартире) (типовые схемы проводки)
О чем еще хотелось сказать, так это о том, что лучше использовать несколько независимых линий питания для каждого из помещений в комнате или квартире. Тем самым вы не будете применять провод с сечением 10 мм 2 для всей квартиры, приброшенный во все комнаты, от которого идут отводы. Такой провод будет приходить на вводный автомат, а затем от него, в соответствии с мощностью потребляемой нагрузки будут разведены выбранные сечения проводов, для каждого из помещений.
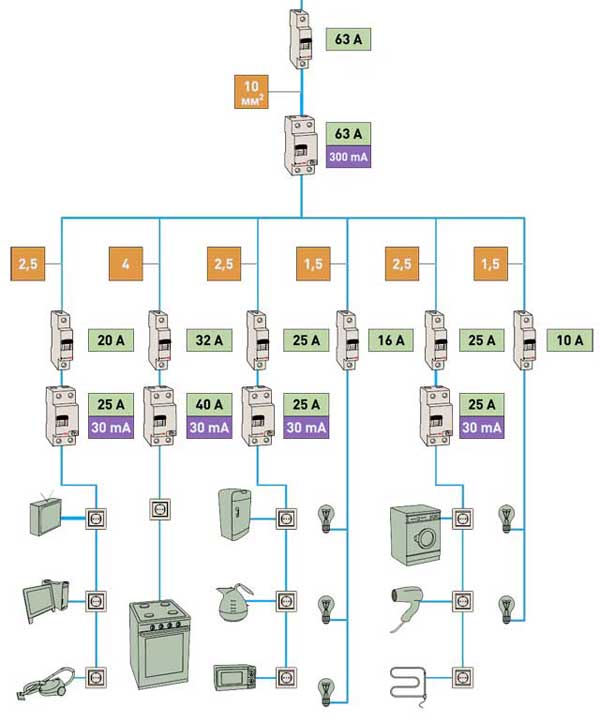
Типовая принципиальная схема электропроводки для квартиры или дома с электрической плитой (с указанием сечения кабеля для электроприборов)
Проводниковые бронзы
Проводниковые бронзы относятся к медным сплавам, необходимость применения которых в основном вызвана недостаточной в ряде случаев механической прочностью и термической устойчивостью чистой меди.
Общая номенклатура бронз весьма обширна, но высокой электропроводностью обладают лишь немногие марки бронз.
· кадмиевая бронза относится к наиболее распространенным проводниковым бронзам. Из числа всех марок кадмиевая бронза обладает наивысшей электрической проводимостью. Вследствие повышенного сопротивления истиранию и более высокой нагревостойкости эта бронза широко применяется для изготовления троллейных проводов и коллекторных пластин;
· бериллиевая бронза относится к сплавам, приобретающим прочность в результате старения. Она обладает высокими упругими свойствами, устойчивыми при нагревании до 250 °C, и электрической проводимостью в 2—2,5 раза большей, чем проводимость других марок бронз общего назначения. Эта бронза нашла широкое применение для изготовления различных пружинных деталей, выполняющих одновременно и роль проводника тока, например: токоведущие пружины, отдельные виды щеткодержателей, скользящие контакты в различных приборах, штепсельные разъемы и т.п.;
· фосфористая бронза обладает высокой прочностью и хорошими пружинными свойствами, из-за малой электропроводности применяется для изготовления пружинных деталей с низкими плотностями тока.
Литые токоведущие детали изготовляются из различных марок машиностроительных литьевых бронз с проводимостью в пределах 8—15% проводимости чистой меди. Характерной особенностью бронз является малая усадка по сравнению с чугуном и сталью и высокие литейные свойства, поэтому они применяются для отливки различных токоведущих деталей сложной конфигурации, предназначенных для электрических машин и аппаратов.
Все марки литьевых бронз можно подразделить на оловянные и безоловянные, где основными легирующими элементами являются Al, Mn, Fe, Pb, Ni.
Какие металлы лучше всего проводят электрический ток и где они используются
Какие металлы лучше всего проводят электрический ток и где они используются
Какой металл лучше всего проводит тепло и электрический ток? Металлы с наивысшей электропроводностью, а также назначение меди, серебра и других токопроводящих материалов.
какой металл лучше проводит, какой металл лучше проводит ток, какой металл лучше проводит электрический, какой металл лучше проводит тепло, какой металл лучше всего проводит электрический ток, какой металл лучше других проводит электрический ток
В этой статье мы рассмотрим, какой металл лучше всего проводит электрический ток. Сразу отметим, что чистые металлы являются более хорошими проводниками по сравнению со сплавами, потому что примеси препятствуют свободному движению электронов.
Наивысшей электропроводностью обладает чистое серебро. Медь немного уступает серебру, но ее большое преимущество – в более низкой стоимости. Благодаря этому в промышленных масштабах используется именно медь.
Золото – хороший проводник, к тому же оно не подвержено окислению. А высокая пластичность позволяет вытянуть сколь угодно тонкую проволоку. Поэтому золото применяется в микроэлектронике. Но недостатком металла является еще более высокая, чем у серебра, стоимость.
Какой металл лучше других проводит электрический ток из числа недорогих материалов? Алюминий. Он уступает предыдущим трем материалам по показателю электропроводности. Но все же он является сильным проводником и устойчив к коррозии. Недостаток алюминия – его повышенная ломкость.
Главное назначение этих материалов – элементы силовых установок, линий электропередач и всех механизмов, связанных с потреблением или передачей электрического тока.
Чаще всего применяются медь и алюминий, а также сплавы: бронзы, латунь. Рассмотрим, какие материалы подходят для производства той или иной продукции.
Медь
Используется только электролитических марок М I, М 0. Она бывает твердой и мягкой.
- Твердая за счет наклепа подходит для коллекторов, проводов.
- Мягкая, после отжига, подходит для производства обмоточных проводов, потому что имеет высокую гибкость.
Латунь
Из нее создаются сложнопрофильные токоведущие детали, которые должны обладать повышенной твердостью и стойкостью к электрическим разрядам.
Алюминий
Подходит для изготовления проводов для линий электропередач, обмоточных и монтажных проводов.
Золото и серебро
Эти дорогие материалы используются в производстве электроники, где их расход относительно небольшой.
Ниже представлена таблица с показателями электропроводности. В ней же видно, какой металл лучше всего проводит тепло.
spb-stal.ru