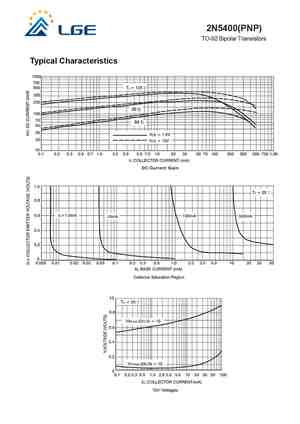
ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ: САМОДЕЛЬНАЯ БАТАРЕЯ
Каждому из нас знакомы химические источники тока различных типов и форм. Но как это часто случается, мы редко задумываемся о том, как устроен этот совершенно привычный и обыденный предмет. А между тем, появление первых химических источников тока, положило начало превращению электричества из лабораторной диковинки в нашего повседневного помощника.
Правильное объяснение этому явлению смог дать другой итальянский ученый Алессандро Вольта. Он установил, что это явление связано с наличием двух разнородных металлов, соприкасающихся с электролитом, в роли которого выступала кровь лягушки, а сама лапка играла лишь роль чувствительного индикатора электрического тока . Опираясь на свои исследования Вольта в 1799г. создал первый химический источник тока. В этом устройстве Вольта использовал медный и цинковый электроды, погруженные в раствор серной кислоты.
Цинк бурно реагирует с кислотами. В раствор переходят не атомы цинка, а положительные ионы, так что в электроде остается избыток электронов, следовательно, цинковая пластина заряжается отрицательно. Вообще, большинство металлов при погружении в электролит заряжается отрицательно, на поверхности медной пластинки протекает подобный процесс. Но избыток отрицательных зарядов на медном электроде гораздо меньше, а значит, относительно цинкового электрода его потенциал получается более высоким. Если соединить внешним проводником медную и цинковую пластины, то электроны начнут перемещаться с цинковой пластины на медную, т.е. в цепи потечет электрический ток .
Часто напряжения, даваемого одним гальваническим элементом, недостаточно. Тогда их можно соединять последовательно в батареи.
Вообще изготовить химический источник тока совсем нетрудно: надо поместить в электролит две пластинки из разных металлов . Такие гальванические элементы возникают самопроизвольно. Например, намочил дождь крышу, покрытую оцинкованным железом, на железе наверняка имеются царапины, так, что и железо, и цинк вступили в контакт с водой, которая играет роль электролита. Цинк в такой паре начнёт активно разрушаться, а вот железо не пострадает, пока не разрушится весь цинк. Именно для этого и покрывают железо слоем цинка.
Нагляднее всего можно пронаблюдать гальваническую коррозию на примере контактов железа с цинком и медью в растворе соли. Железные скрепки были надеты на цинковую и медную пластины и погружены в раствор соли.
Через сутки скрепка, соединенная с медной пластиной, покрылась ржавчиной. В то время, как скрепка, бывшая в контакте с цинком, совершенно не пострадала.
Ученые составили электрохимический ряд напряжений металлов. Чем дальше друг от друга отстоят металлы в этом ряду, тем более высокое напряжение дает гальванический элемент, составленный из этих металлов. Так пара золото – литий теоретически может дать электродвижущую силу (ЭДС) 4,72 В. Но такая пара в водной среде работать не сможет – литий это щелочной металл, легко реагирующий с водой, а золото стоит слишком дорого для подобного применения.
На практике элемент Вольта обладает рядом серьёзных недостатков.
- Во-первых, электролитом ему служит весьма едкая жидкость – раствор серной кислоты. Жидкий электролит всегда представляет собой неудобство или даже опасность. Он может расплескаться, разлиться при повреждении корпуса.
- Во-вторых, на медном электроде такого элемента будет выделяться водород. Это явление называется поляризацией. По многим свойствам водород весьма близок к металлам, так что его пузырьки создадут дополнительную ЭДС поляризации, стремящейся вызвать ток противоположного направления . Кроме того, пузырьки газа не пропускают электрический ток, что тоже ведет к ослаблению тока. Поэтому приходится периодически встряхивать сосуд, удаляя пузырьки механически, или вводя в состав электролита специальные деполяризаторы.
- В третьих, в процессе работы гальванического элемента Вольта, цинковый электрод постепенно растворяется. Теоретически, когда гальванический элемент не используют, разрушение цинкового электрода должно прекратиться, но поскольку почти всегда в составе цинка есть примеси других металлов, они при соприкосновении с электролитом играют роль второго электрода, образуя короткозамкнутый элемент, что ведет к гальванической коррозии цинкового электрода . Для того, чтобы устранить этот недостаток, приходится использовать сверхчистый цинк или конструктивно предусматривать возможность извлечения цинкового электрода из электролита. Так что когда батарея не используется, электролит из нее следует сливать.
Но для демонстрационных целей всеми этими недостатками можно пренебречь, если заменить серную кислоту более безопасным электролитом.
Понятие об электролизе. Принципиальная схема электролизера.
Гальваника — это осаждение металла или оксида на поверхности изделия для придания ему новых функциональных свойств или улучшения внешнего вида. Гальваника выполняется под действием электрического тока, отсюда возникает понятие «электролиз».
Электролиз с практической точки зрения является комплексом окислительно-восстановительных реакций, протекающих под действием электрического тока в электролите.
Электролит — это среда (для классической гальваники — водный раствор), обладающая ионной электрической проводимостью. Проще говоря — жидкость, способная проводить через себя электрический ток. Электрический ток проводится в основном за счет сольватированных в растворителе ионов. Сольватация является своего рода «растаскиванием» ионов из прочной кристаллической решетки твердого вещества диполями воды. В результате каждый ион становится окружен некоторым количеством молекул воды и в этом виде передвигается либо к положительному, либо к отрицательному электроду.
Когда через электролит пропускается электрический ток, то первоначально происходит направленное движение электронов в металлических проводниках. От анода электроны переходят к катоду, в результате чего на аноде образуется избыточный положительный заряд. При включенной электрической цепи с внешним источником тока на растворимом аноде будет происходить отнятие электронов у атомов металла-основы анода, а на нерастворимом — отнятие электронов у тех анионов, которые находятся прианодной области. На катоде же появляется избыточный отрицательный заряд за счет скопившихся на нем электронов. К положительному аноду начинают движение противоположно заряженные анионы, а к катоду — катионы. При этом достигнув электродов они могут претерпевать определенные химические превращения.
Проходящий через электролит ток обычно постоянный, хотя иногда он может быть и переменным или изменяться по определенной функции. В любом случае, мы всегда сможем выделить катодный (восстановление) и анодный (окисление) процессы.
Электролиз не обязательно должен происходить только в водных растворах. Существуют также неводные электрохимические системы на основе органических (в основном апротонных) растворителей, солевых расплавов и даже твердых электролитов, однако их применение в промышленности для получения металлических покрытий ограничено, а в случае твердых электролитов — вообще невозможно.
В гальванике, исходя из вышеприведенной схемы, может быть три варианта организации процесса:1. Электролиз с растворимыми анодами. Металл анода растворяется и его ионы переходят в раствор, а на катоде эти же ионы восстанавливаются и осаждается металлическое покрытие. Примеры такого процесса — цинкование, меднение, никелирование и т.п.
2. Электролиз с нерастворимыми анодами. Анод не растворяется, на нем происходит побочная реакция, например, выделение кислорода. На катоде происходит восстановление металла, ионы которого подтягиваются из электролита. Происходит непрерывное снижение концентрации ионов металла в растворе.
3. Анодирование — получение оксидного покрытия на детали, завешенной в ванну анодом, на катоде идет выделение водорода.Устройство для проведения электролиза называется электролизером. Небольшой лабораторный электролизер принято называть ячейкой, в то время как промышленная установка будет называться гальванической ванной.
Схема простейшего электролизера (рисунок 1 и 2) всегда включает в себя:
• электролит, через который протекает электрический ток;
• катод(ы) — покрываемые детали (отрицательный электрический полюс, на котором происходит процесс принятия электронов — восстановления).
• Катод, на который наносится покрытие также может называться подложкой или основой, а покрытие на катоде — осадком;
• аноды — противоэлектроды (положительный электрический полюс, на котором происходит процесс отдачи электронов — окисления);
• источник электрического тока.
В случае нанесения анодного оксидного покрытия, например, на алюминии (процесс анодирования), покрываемые изделия находятся на аноде, а катоды выполняют роль противоэлектродов.
Электролизер может комплектоваться и дополнительным оборудованием:• нагреватели; • системы перемешивания; • системы фильтрации;• бортовые отсосы;• крышки;• датчики технологических параметров (температуры, рН, уровень, потенциал, концентрация компонентов и т.п.), дозаторы и другие средства автоматизации.
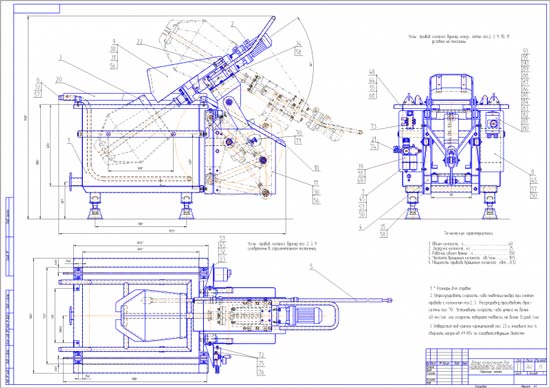
Рисунок 1 — Принципиальная схема электролизера
Рисунок 2 — Реальный электролизер (гальваническая ванна блестящего цинкования из щелочного цинкатного электролита).
Обработка готового изделия
Гальваническое покрытие деталей завершается этапом дополнительной обработки. В этом процессе реализуются следующие операции:
- Осветление.
- Окраска лакокрасочными составами.
- Пассивирование.
- Обезводороживание.
- Промасливание или полировка.
- Выполнение серебрения составами против тусклости.
Осветление и пассивирование повышают антикоррозионные свойства оцинкованных изделий и кадмиевых покрытий. Процесс пассивирования – это погружение изделий в специальный раствор, образующий на поверхности детали защитную пленку толщиной до 1 мкм.
Изделия из стали, меди с гальваническим покрытием дополнительно обрабатывают маслами – промасливают. Это делается в целях улучшения защитных качеств металлической изоляции и способствует повышению антикоррозионной устойчивости.

Что такое гальваника?
Гальваника – это процесс, в котором используется электрический ток, чтобы уменьшить растворенные катионы металла настолько, что они образуют единое покрытие на металле электрода. Этот термин также применяется для характеристики электрических окислений из анионов на твердой подложке, например, в формировании хлорида серебра на серебряной проволоке, хлоридно-серебреные электроды. Гальваника в основном используется для изменения свойств поверхности объекта:
- Устранения физических повреждений и увеличения износостойкости;
- Повышения защиты от коррозии, снижения уровня скольжения;
- Улучшения эстетических качеств;
- Также гальванические процессы применяются для увеличения толщины на низкорослых частях объекта или формирования плотностей.
Процесс, в котором используется гальваническое травление, называется электроосаждением. Он противоположен гальваническому воздействию. С его помощью можно осуществить как электроочистку детали, так и нанести на нее гальваническое покрытие. Это зависит от того, к чему подключается деталь (к аноду или катоду). Емкость гальванической ванны наполняется электролитом, содержащим одну или несколько растворенных солей металлов, что увеличивает прохождение электрического тока и способствует образованию ионов.
После того, как постоянный ток подключен к аноду, составляющие его атомы металла окисляются и растворяются в электролите. На катоде наблюдается обратный процесс – растворенные ионы металла начинают осаждаться, образовывая покрытие. Скорость, с которой растворяется анод, зависит от площади поверхности катода, по которой движется электрический ток. Таким образом работают гальванические четырехкамерные автоматизированные ванны.
Чем дольше объект остается в электрической среде ванны, тем толще станет слой покрытия. Например, после гальванического воздействия позолоченный металлический слой может быть толщиной от 10 мкм для настоящего золота и 20 мкм или более для посеребренных приборов.
Форма и контур объекта может повлиять на толщину покрытия. Металлические предметы, имеющие острые углы и ребра, как правило, имеют более толстое покрытие на углах и более тонкое в углублениях. Это происходит потому, что постоянный ток протекает более плотно вокруг внешнего края объекта, чем в углублениях. Такие предметы, как часы с острыми гранеными углами, перстни, трудно обработать равномерно. Из-за такого соответствия приходится использовать разные уровни тока и углы воздействия.

За редким исключением, гальванические процессы не смогут скрыть существовавшие ранее дефекты поверхности (например, царапины и вмятины), напротив, они даже могут их сделать более заметными. Поэтому необходимо затереть или обработать физическими методами любую поверхность перед нанесением покрытия.
В результате гальванического воздействия внутренняя структура материала остается неизменной. Для глубинного воздействия используются различные технологии, например, химические методики, дробеструйное производство и прочее.
Самодельная батарейка из подручных средств
Батарейка или гальванический элемент – это химический источник электрического тока. Все батарейки, продающиеся в магазинах, по сути, имеют одинаковую конструкцию. В них используются два электрода из разного состава. Основным элементом для отрицательного вывода (анода) солевых и щелочных батареек является цинк, а для их положительного (катода) – марганец. Катод литиевых батареек изготавливается из лития, а для анода используются самые различные материалы.
Между электродами батареек расположен электролит. Состав его различен: для солевых батареек, имеющих самый низкий ресурс, используется хлорид аммония. Для изготовления щелочных батареек применяют гидроксид калия, а в литиевых батарейках используется органический электролит.
https://youtube.com/watch?v=chfVwKF5R1A
При взаимодействии электролита с анодом вблизи него образуется избыток электронов, создающий разность потенциалов между электродами. При замыкании электрической цепи количество электронов за счет химической реакции постоянно пополняется, и батарейка поддерживает протекание тока через нагрузку. При этом материал анода постепенно коррозирует и разрушается. При полной его выработке ресурс батарейки оказывается исчерпан.
Несмотря на то, что состав батареек сбалансирован производителями для обеспечения долгой и стабильной их работы, изготовить элемент питания можно и самому. Рассмотрим несколько способов, как можно сделать батарейку своими руками.
Методы гальваники
Формирование защитной пленки посредством распределения другого металла выполняется с помощью 2 технологий:
- Катодное напыление. При незначительном повреждении слоя происходит образование ржавчины на основном изделии. Это связано с реакцией самого поверхностного покрытия.
- Анодное нанесение. Метод характеризуется большей эффективностью в сравнении с предыдущим вариантом. Если появляется угроза развития коррозийных процессов, то они происходят только в поверхностном слое. Основная часть изделия долго не теряет начальных внешних свойств. Кроме того, материал остается защищенным от негативных воздействий окружающей среды.
Особенности гальванизации с различными металлами дома
Ниже приведены нюансы, которые следует учитывать при воспроизведении отдельных технологий.
Никелирование металлических изделий
Для этого процесса применяют повышение температуры (от +24°C до +26°C) и гальванического тока до 1,2 А на дм кв., по сравнению с представленным выше серебрением. Тщательно контролируют водородный показатель. Рекомендованный диапазон pH – от 3 до 6. Прочный слой успеет образоваться за 30-40 мин.
Покрытие медью без погружения
Изделие из стали закрепляют в держателе, подключают к источнику постоянного тока (минус). Кисточку, сделанную из многожильного медного провода, обмакивают в электролит. Этот инструмент подключают к плюсу. Им водят по обрабатываемой части поверхности.
Электрохимическое цинкование
Электролит создают из следующих ингредиентов:
- дистиллированная вода – 2 литра;
- сернокислый аммоний – 100 г.;
- сернокислый цинк – 400 г.;
- натрий уксусный – 30 г.
Обработка длительностью 30-40 минут создаст прочный слой, хорошо защищающий детали от коррозии. Этот способ дешевле, чем применение аналогичных деталей из нержавеющей стали.
Хромирование изделий из металла
Для надежности этот слой закрепляют на технологической подложке из никеля. Такое решение не образует гальваническую пару. Повышением температуры увеличивают блеск декоративного покрытия. Прочные покрытия получают при плотности тока более 90 А на дм кв., что сложно обеспечить в домашних условиях.
Толщина серебрения в зависимости от условий эксплуатации и назначения деталей
Серебро отличается устойчивостью к щелочным растворам и большинству органических кислот, концентрированная серная кислота может растворять металл только при кипячении, а соляная при значительном нагревании. Под воздействием аммиака и хлора на поверхности серебра образуется тонкая пленка, повышающая значения сопротивлений и затрудняющая процесс пайки, металл теряет свои преимущества. Для предупреждения негативных явлений применяется специальная технология финишной обработки.
Особые физико-химические характеристики покрытия определяют метод серебрения и конкретную область использования покрытий, покрытие широко распространено вне зависимости от высокой стоимости и дефицитности металла. Серебрение изделий применяется для повышения отражательных характеристик оптических и светотехнических приборов, для понижения переходного сопротивления и деталей, контактирующих между собой, для повышений устойчивости к коррозионным процессам и в декоративных целях при изготовлении ювелирных изделий.
Как работают такие батареи
В основе работы бета-гальванических батарей лежит принцип преобразования альфа- и бета-излучений радиоактивного вещества в обычный электрический ток, питающий всю современную технику. Как заверил Нима Голшарифи, созданным компанией источникам энергии можно придавать практически любую форму, другими словами, их можно выпускать в виде привычных многим батареек различных форматов – АА, 18650, CR2032 и др.
Батарейка Nano Diamond Battery может работать тысячелетиями
Конструкция бета-гальванической батареи состоит в первую очередь из радиоактивного сердечника, который выступает в качестве источника изотопов. Нима Голшарифи подчеркнул, что сердечник изготавливается из небольшого количества переработанных ядерных отходов.
Для того чтобы сделать батареи безвредными для людей и окружающей среды, специалисты Nano Diamond Battery покрыли «фонящий» сердечник специальными нерадиоактивными синтетическими алмазами, выращенными в лабораторных условиях. Это очень дешевые в производстве аналоги обычных алмазов.
Изотопы радиоактивного элемента в процессе так называемого «неупругого рассеяния» взаимодействуют с алмазным покрытием, и в итоге энергия бета-излучения преобразуется в электрический ток.
Для чего нужна «вечная» батарея
Столь значительный период работы батарей разработчики объяснили тем, что используемое в качестве сердечника вещество может оставаться радиоактивным сотни и тысячи лет. Они отметили также, что такие батареи могут вырабатывать чрезмерно большое количество энергии, которую они предлагают хранить в дополнительной «буферной» емкости. В качестве такой емкости могут служить суперконденсаторы, а в России, как сообщал CNews, как раз научились изготавливать их из бесполезного сорного растения – борщевика.
Методы гальваники
Формирование защитной пленки посредством распределения другого металла выполняется с помощью 2 технологий:
- Катодное напыление. При незначительном повреждении слоя происходит образование ржавчины на основном изделии. Это связано с реакцией самого поверхностного покрытия.
- Анодное нанесение. Метод характеризуется большей эффективностью в сравнении с предыдущим вариантом. Если появляется угроза развития коррозийных процессов, то они происходят только в поверхностном слое. Основная часть изделия долго не теряет начальных внешних свойств. Кроме того, материал остается защищенным от негативных воздействий окружающей среды.
Одновременное протекание реакций на электроде. Выделение металла одновременно с газом. Сплавообразование.
Случаи, когда при нанесении гальванического покрытия на электроде протекает только одна реакция довольно редки. Гораздо чаще происходит одновременно две и более реакции. Условием для одновременного протекания двух электрохимических процессов является максимальное сближение потенциалов их разряда. Можно классифицировать ситуации следующим образом:• Восстановление (осаждение) металла одновременно с выделением водорода;• Восстановление (осаждение) металла одновременно с одним или несколькими другими металлами, а также, иногда, неметаллами и органическими веществами.
Также в качестве побочных реакций могут выступать реакции неполного восстановления металла (Fe3+ → Fe2+), реакции восстановления оксидных пленок и т.п.
Как правило, все процессы осаждения металлов в гальванике идут с одновременным восстановлением примесей из раствора (посторонние металлы, сера, органика и т.п.), продукты восстановления которых встраиваются в покрытие и вызывают изменение его физико-механических свойств — положительное или отрицательное. Примером положительно влияющей примеси (можно назвать ее легирующим компонентом) является висмут в сплаве олово-висмут, дающий улучшение коррозионной стойкости, предотвращение эффекта «оловянной чумы», увеличение срока сохранения способности к пайке. Примером сплава с вредной примесью — никелевое покрытие, загрязненное медью (медь дает ухудшение прочности сцепления покрытия с основой, ухудшение внешнего вида — потерю блеска, образование грязно-серого покрытия, ухудшение защитных антикоррозионных свойств).
6.1 Выделение водорода одновременно с осаждением металла на катоде.
Выделение водорода одновременно с покрытием происходит, например, при никелировании, хромировании, цинковании из цинкатного электролита, лужении из кислого электролита и т.д. Выделение водорода усиливается при приближении к предельному диффузионному току.
Рассмотрим рисунок 8, на котором показаны поляризационные кривые одновременного выделения водорода и металла на катоде. При потенциале Е1 доля общего тока, приходящегося на выделение металла составляет примерно 2/3 общего тока, а выделения водорода — 1/3. При более отрицательном потенциале Е2 наоборот, доля тока осаждения металла составит 1/3 общего, а доля тока выделения водорода — 2/3. И чем более отрицательный потенциал мы будем задавать, тем больше будет доля тока выделения водорода в общей величине тока, пропущенного через электролизер.
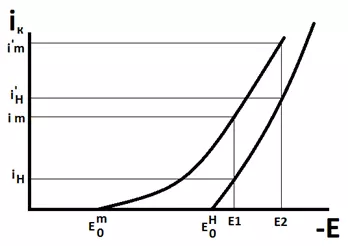
Рисунок 8 — Поляризационные кривые одновременного выделения металла и водорода. Выделение водорода при катодном осаждении металла практически всегда отрицательно сказывается на качестве покрытия. Тому есть несколько причин:• Водород может проникать в покрытие и металлическую основу, вызывая «водородную хрупкость» металлов.• Водород может задерживаться на поверхности металла, вследствие чего покрытие будет расти вокруг пузырька газа. В результате будет образовываться ямочка, иногда доходящая до подложки — «питтинг». Это особенно актуально для никелирования.

Рисунок 9 — Схема образования питтинга за счет пузырька водорода, прилипшего к покрытию• Водород может создавать «газовые мешки», под которыми покрытия образовываться не будет (рисунок 10).
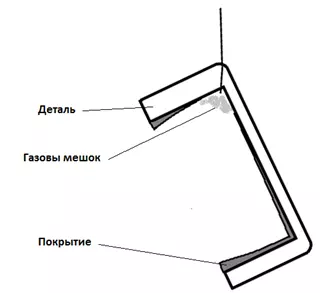
Рисунок 10 — Схема образования газовых мешков.С другой стороны, очень редко водород может играть и положительную роль, например при щелочном цинковании из цинкатного электролита. Обильное выделение водорода в этом процессе позволяет доочистить поверхность покрываемых деталей от загрязнений и несколько улучшить прочность сцепления покрытия с основой в этом случае (здесь речь будет идти об «очищающем» действии электролита). Однако, не следует забывать и о том, что обильное выделение водорода одновременно с этим ухудшит физико-механические свойства покрытия за счет наводораживания и, соответственно, водородной хрупкости. Кроме этого, десорбирующийся из детали водород при сильно напряженном покрытии может вызывать появление отслоений в виде пузырей.